طی قرون گذشته، ترکیبات مولکولی قهوه برشته شده از طریق تقطیر و کروماتوگرافی مشخص شده اند. این ترکیبات طیف پیچیده ای از مولکول های آلی پس از برشته شدن را تشکیل می دهند که از نظر طعم و شدت متفاوت هستند. این مطالعات، تحقیقات هماهنگی را در دانشگاه ها و موسسات خصوصی برای دستیابی این طعم ها در یک فنجان قهوه متعادل و خوشمزه برانگیخت. با این حال، متغیرهای زیادی برعصارهگیری ترکیبات قهوه در آب تأثیر میگذارند. برشته کاری، اندازه آسیاب، دما، فشار و زمان دم آوری، محصول فنجان را تعریف میکند، اما این آب است که عصارهگیری قندها، نشاسته ها، بازها و اسیدها را تسهیل میکند.


خرید قهوه رئیس بلند، انتخاب اول کافهها!
دانههای مرغوب آمریکای لاتین در این ترکیب طوری انتخاب شدهاند که عطر عمیق، کرمای جذاب و طعمی بالانسشده ایجاد کنند؛ دقیقا همان چیزی که مشتری بعد از یک بار چشیدن، دوباره میخواهد تجربهاش کند.
اگر به دنبال یک قهوه اقتصادی، پایدار و مناسب برای مصرف روزانه در کافه هستید، وقتشه قهوه رئیس بلند رو تست کنید و تفاوت رو ببینید.
نقش آب و ناخالصیهای آن بهطور تجربی با جزئیات بسیار مورد بررسی قرار گرفته است، در دو مطالعه جداگانه که در ابتدا توسط لاکهارت و همکاران و بعداً توسط پنگبورن و همکاران انجام شد. همراه با اثرات جالب بر عصارهگیری قهوه، هر دو مطالعه نیز نقشی که ناخالصی های آب هم در طعم و هم در رنگ آب، قبل از عصارهگیری بازی می کنند را توصیف میکنند. با این حال، این آثار منحصر به متغیرهای معمولی که صنعت قهوه را آزار میدهند، نبودند: یونهای محلول دیگر مانند فلزات رسانا، هالیدها، نیترات، سولفات، فسفات، و مهمتر از همه، کربنات. نقش یون های محلول در عصارهگیری ترکیبات قهوه برای تعیین کمیت آزمایشی چالش برانگیز است، زیرا برهمکنش های رقابتی زیادی وجود دارد که هم از نظر آنتروپی و هم از نظر ترمودینامیکی مهم هستند (به عنوان مثال، جابجایی آب از کره های یکسان برای تشکیل جفت یون).
انحلال مولکول های بزرگتر، پیچیده تر است، زیرا املاح اغلب دارای آرایه پیچیده ای از نقش های قطبی اند. در شیمی طعم، اجزای آلی دارای نواحی آبدوست و آبگریز رقابتی هستند که از طریق پیوند هیدروژنی، برهمکنشهای کولمبیک و از طریق تشکیل قفسهای هیدرات منظم با آب تعامل دارند. صرف نظر از این، زمانی که املاح زیر نقطه اشباع آب هستند، به طور قابل توجهی پیوند الکترواستاتیک یا هیدروژنی سیستم حجیم را تغییر نمی دهند. در تایید تحقیقات انجام شده توسط لاکهارت، حد بالایی یون های محلول در عصارهگیری قهوه توسط اشباع محدود نمی شود، بلکه با عصارهگیری بیش از حد محدود می شود. در این زمینه، ما به دنبال نقشی که کاتیون های محلول در عصارهگیری ترکیبات قهوه ایفا می کنند هستیم.
د ر تلاشی برای ساده کردن مشکل برای کاربر نهایی، انجمن تخصصی قهوه اروپا (SCAE) دستورالعملهایی درباره آب «ایدهآل» برای عصارهگیری قهوه ابداع کرد. این رهنمودها در صنعت قهوه درست هستند. کمی کردن تمام یون های محلول طبیعتا مجموع هر دو غلظت کاتیونی و آنیونی از طریق اندازه گیری هدایت یونی کل جامدات محلول (TDS) به دست می آید. در نتیجه، SCAE محدودهای نامشخص با محدودیت مواد جامد محلول (حدود ppm 300 (را برای عصارهگیری مطلوب قهوه پیشنهاد میکند. در بیشتر نقاط جغرافیایی غلظت بی کربنات بیشتر از فلزات قلیایی خاکی محلول است و در نتیجه آب دارای قابلیت بافر بالا است. با در نظر گرفتن دستورالعمل حد اکثر ppm 300 ، تولیدکنندگان عمده تصفیه آب و تبادل یونی بر حذف یا تبادل CO32- محلول تمرکز میکنند، که ذاتاً Ca2+ را از طریق ترکیب دوباره کاهش میدهند، تشکیل رسوب، و در مجموع TDS را کاهش میدهد. واحدهای تصفیه معمولی یا دارای یک سیستم اسمزی هستند یا ذرات را روی یک بلوک کربن فیلتر می کنند، در حالی که واحدهای مبادله عموما دارای یک کانال بافر کربوکسیلاتی Mg2+ یا Na+هستند که به طور همزمان غلظت Ca2+ را از طریق تبادل یون و مقداری کربنات (به عنوان CO2) از طریق ستون حل شده به سرعت کاهش می دهد. با توجه به رویکرد صنعتی کنونی، انتقال پروتون املاح و دکربوکسیلاسیون بعدی ، به نظر میرسد یونهای محلول به جای مهار کردن، باید مدیریت و کاهش یابند.
برهمکنش بین یون محلول و آب، وابسته به گونه است. برای مثال، هیدراتاسیون Ca2+ گرمازاتر از Mg2+ است.
استفاده از شیمی محاسباتی معاصر ابزار مفیدی برای مطالعه چنین مباحثی است. در اینجا ما یک رویکرد شیمیایی کوانتومی قابل دسترس برای تعیین کمیت اتصال مواد آلی قهوه به یونهای فلزی محلول آشنا، Na+، Mg2+ و Ca2+ پیشنهاد میکنیم. ما پنج نمونه اولیه اسید (1-5)، کافئین (6) و اوژنول (7) را به عنوان نمایندگان دسته بزرگتری از مشتقات آلی که در غلظت های مختلف در دانه برشته شده یافت می شوند انتخاب کرده ایم. (شکل 1). از بین پنج اسید، اسیدهای لاکتیک (1) و مالیک (2) نتهای ترش را در خود جای میدهند، در حالی که اسید سیتریک (3) طعم شیرین جذابی دارد. اسید کوینیک (4) و مشتق بزرگتر آن اسید کلروژنیک (5) طعمی تند و ناخوشایند در نظر گرفته می شود. کافئین (6) به عنوان یک نمونه اولیه آلکالوئید معطر (و دارای باز ضعیف، pKa = 14) گنجانده شده است، در حالی که اوژنول (7) دارای یک نت چوبی لذت بخش است که در قهوه، شراب و ویسکی یافت می شود. لازم به ذکر است که برخی از اسیدها به عنوان نمک پتاسیم در دانه ها وجود دارند. همانطور که در ادامه این مقاله بحث خواهیم کرد، K+ اتصال بسیار ضعیفتری به اجزای قهوه نشان میدهد، زیرا هم پراکنده است و هم به تنهایی شارژ میشود. در اینجا، ما اسیدها را به شکل اسید آزاد آنها در نظر می گیریم، زیرا انرژی های اتصال نسبی مولکول های خنثی که با یون ها هماهنگ می شوند، ضعیف ترین برهمکنش های ممکن را نشان می دهند، که اهمیت گونه های یونی را برجسته می کند.
شکل 1. هفت ترکیب موجود در قهوه برشته شده که طیف وسیع عملکرد را نشان می دهد. پنج اسید کربوکسیلیک در افزایش وزن مولکولی وجود دارد: اسید لاکتیک (1)، اسید مالیک (2)، اسید سیتریک (3)، اسید کوئینیک (4)، اسید کلروژنیک (5)، یک آلکالوئید، کافئین (6)، و یک نت طعم، اوژنول (7).
سفارش قهوه کیلویی و عمده از کافه رئیس
کافه رئیس با تجربه چندین ساله در زمینه رست و عرضه بهترین دانههای قهوه از سراسر دنیا و استفاده از جدیدترین تجهیزات و تکنولوژی، آماده ارائه قهوه با کیفیت و قیمت مناسب به شماست. همین حالا کلیک کنید و قهوه مورد علاقه خود را سفارش دهید.
نقش آب و ناخالصیهای آن بهطور تجربی با جزئیات بسیار مورد بررسی قرار گرفته است، در دو مطالعه جداگانه که در ابتدا توسط لاکهارت و همکاران و بعداً توسط پنگبورن و همکاران انجام شد. همراه با اثرات جالب بر عصارهگیری قهوه، هر دو مطالعه نیز نقشی که ناخالصی های آب هم در طعم و هم در رنگ آب، قبل از عصارهگیری بازی می کنند را توصیف میکنند. با این حال، این آثار منحصر به متغیرهای معمولی که صنعت قهوه را آزار میدهند، نبودند: یونهای محلول دیگر مانند فلزات رسانا، هالیدها، نیترات، سولفات، فسفات، و مهمتر از همه، کربنات. نقش یون های محلول در عصارهگیری ترکیبات قهوه برای تعیین کمیت آزمایشی چالش برانگیز است، زیرا برهمکنش های رقابتی زیادی وجود دارد که هم از نظر آنتروپی و هم از نظر ترمودینامیکی مهم هستند (به عنوان مثال، جابجایی آب از کره های یکسان برای تشکیل جفت یون).
در تلاشی برای ساده کردن مشکل برای کاربر نهایی، انجمن تخصصی قهوه اروپا (SCAE) دستورالعملهایی درباره آب «ایدهآل» برای عصارهگیری قهوه ابداع کرد. این رهنمودها در صنعت قهوه درست هستند. کمی کردن تمام یون های محلول طبیعتا مجموع هر دو غلظت کاتیونی و آنیونی از طریق اندازه گیری هدایت یونی کل جامدات محلول (TDS) به دست می آید. در نتیجه، SCAE محدودهای نامشخص با محدودیت مواد جامد محلول (حدود ppm 300 (را برای عصارهگیری مطلوب قهوه پیشنهاد میکند. در بیشتر نقاط جغرافیایی غلظت بی کربنات بیشتر از فلزات قلیایی خاکی محلول است و در نتیجه آب دارای قابلیت بافر بالا است. با در نظر گرفتن دستورالعمل حد اکثر ppm 300 ، تولیدکنندگان عمده تصفیه آب و تبادل یونی بر حذف یا تبادل CO32- محلول تمرکز میکنند، که ذاتاً Ca2+ را از طریق ترکیب دوباره کاهش میدهند، تشکیل رسوب، و در مجموع TDS را کاهش میدهد. واحدهای تصفیه معمولی یا دارای یک سیستم اسمزی هستند یا ذرات را روی یک بلوک کربن فیلتر می کنند، در حالی که واحدهای مبادله عموما دارای یک کانال بافر کربوکسیلاتی Mg2+ یا Na+هستند که به طور همزمان غلظت Ca2+ را از طریق تبادل یون و مقداری کربنات (به عنوان CO2) از طریق ستون حل شده به سرعت کاهش می دهد. با توجه به رویکرد صنعتی کنونی، انتقال پروتون املاح و دکربوکسیلاسیون بعدی ، به نظر میرسد یونهای محلول به جای مهار کردن، باید مدیریت و کاهش یابند.
برهمکنش بین یون محلول و آب، وابسته به گونه است. برای مثال، هیدراتاسیون Ca2+ گرمازاتر از Mg2+ است.
انحلال مولکول های بزرگتر، پیچیده تر است، زیرا املاح اغلب دارای آرایه پیچیده ای از نقش های قطبی اند. در شیمی طعم، اجزای آلی دارای نواحی آبدوست و آبگریز رقابتی هستند که از طریق پیوند هیدروژنی، برهمکنشهای کولمبیک و از طریق تشکیل قفسهای هیدرات منظم با آب تعامل دارند. صرف نظر از این، زمانی که املاح زیر نقطه اشباع آب هستند، به طور قابل توجهی پیوند الکترواستاتیک یا هیدروژنی سیستم حجیم را تغییر نمی دهند. در تایید تحقیقات انجام شده توسط لاکهارت، حد بالایی یون های محلول در عصارهگیری قهوه توسط اشباع محدود نمی شود، بلکه با عصارهگیری بیش از حد محدود می شود. در این زمینه، ما به دنبال نقشی که کاتیون های محلول در عصارهگیری ترکیبات قهوه ایفا می کنند هستیم.
استفاده از شیمی محاسباتی معاصر ابزار مفیدی برای مطالعه چنین مباحثی است. در اینجا ما یک رویکرد شیمیایی کوانتومی قابل دسترس برای تعیین کمیت اتصال مواد آلی قهوه به یونهای فلزی محلول آشنا، Na+، Mg2+ و Ca2+ پیشنهاد میکنیم. ما پنج نمونه اولیه اسید (1-5)، کافئین (6) و اوژنول (7) را به عنوان نمایندگان دسته بزرگتری از مشتقات آلی که در غلظت های مختلف در دانه برشته شده یافت می شوند انتخاب کرده ایم. (شکل 1). از بین پنج اسید، اسیدهای لاکتیک (1) و مالیک (2) نتهای ترش را در خود جای میدهند، در حالی که اسید سیتریک (3) طعم شیرین جذابی دارد. اسید کوینیک (4) و مشتق بزرگتر آن اسید کلروژنیک (5) طعمی تند و ناخوشایند در نظر گرفته می شود. کافئین (6) به عنوان یک نمونه اولیه آلکالوئید معطر (و دارای باز ضعیف، pKa = 14) گنجانده شده است، در حالی که اوژنول (7) دارای یک نت چوبی لذت بخش است که در قهوه، شراب و ویسکی یافت می شود. لازم به ذکر است که برخی از اسیدها به عنوان نمک پتاسیم در دانه ها وجود دارند. همانطور که در ادامه این مقاله بحث خواهیم کرد، K+ اتصال بسیار ضعیفتری به اجزای قهوه نشان میدهد، زیرا هم پراکنده است و هم به تنهایی شارژ میشود. در اینجا، ما اسیدها را به شکل اسید آزاد آنها در نظر می گیریم، زیرا انرژی های اتصال نسبی مولکول های خنثی که با یون ها هماهنگ می شوند، ضعیف ترین برهمکنش های ممکن را نشان می دهند، که اهمیت گونه های یونی را برجسته می کند.
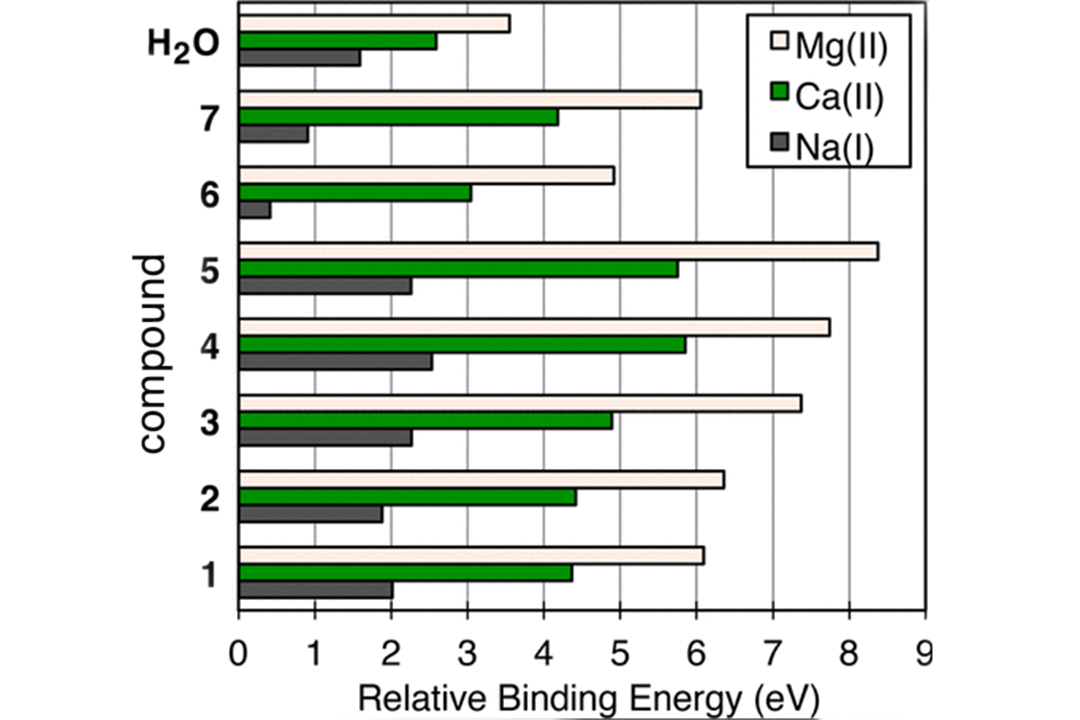
انرژی اتصال نسبی (1-7) – Mg2+ در همه موارد بالاترین است، با ET متناسب با چگالی بار ترکیبات 1-7 Mg2+-آب غنی است اگر افزایش بازده عصارهگیری مهم باشد. با این حال، یک افزایش ظریف اما مهم در انرژی اتصال نسبی 1-3 نسبت به 4 و 5 به Mg2+ در مقایسه با Ca2+ (اگر فقط تقریباً 5٪) وجود دارد. این مطلوب است، و نشان می دهد که آب غنی از Mg2+ به مقدار کمی بیشتر از طعم های مطلوب در قهوه متصل می شود، اگرچه اثرات ماکروسکوپی آن به صورت تجربی بهتر قابل بررسی است. انرژی های اتصال بالای اسیدهای نامطلوب 4 و 5 کمتر خوشایند است. نسبت به سایر یون ها، Mg2+ به طور قابل توجهی عصارهگیری این ترکیبات را افزایش می دهد، که ممکن است اثراتی برای سلامت مصرف کننده و لذت بردن او از فنجان داشته باشد. در این مورد، اهمیت کربنات محلول و سایر بازها مهم است. بیکربنات/کربنات به شدت با 5 (pKa = 2.66) برهمکنش می کند، مقداری از این اسید کمتر مطلوب را خنثی می کند، در مقابل برهمکنش با اسیدهای کوچکتر، 1-3 ( pKa به ترتیب 3.86، 3.40، و 3.14). این تعامل خارج از محدوده این مقاله است، اما مطمئناً مهم است و جهتی است که در آینده قصد بررسی آن را داریم روند اتصال مشابه برای های Ca2+ مشاهده شده است. با این حال، انرژی اتصال نسبی کمتر از Mg2+در همه موارد است.
انرژی اتصال 6- Ca2+ با H2O-Ca2+ قابل مقایسه است. این تنها موردی است که در آن یکی از کاتیون های دو ظرفیتی به طور ضعیف با یک موتیف غنی از الکترون برهمکنش می کند. این یک نتیجه شگفتانگیز نیست زیرا چگالی الکترونی کافئین در سراسر موتیف معطر مزدوج تغییر مکان داده میشود، که منجر به انرژیهای اتصال کم به تمام یونهای فلزی میشود (در مورد Na+، تقریباً غیرتعاملی). با توجه به نتایج جدول 1، انرژی های اتصال آشکارا متناسب با بار و نسبت معکوس با شعاع یونی هستند. بنابراین ما نیازی به بررسی اتصال K+ نداریم زیرا پیشبینی میشود که ET حتی کمتر از Na+باشد. بنابراین، K+ موجود در دانه ها، اگر ناپایدار نباشد میتواند به شکل نمک بسیار ضعیف در نظر گرفته شود.
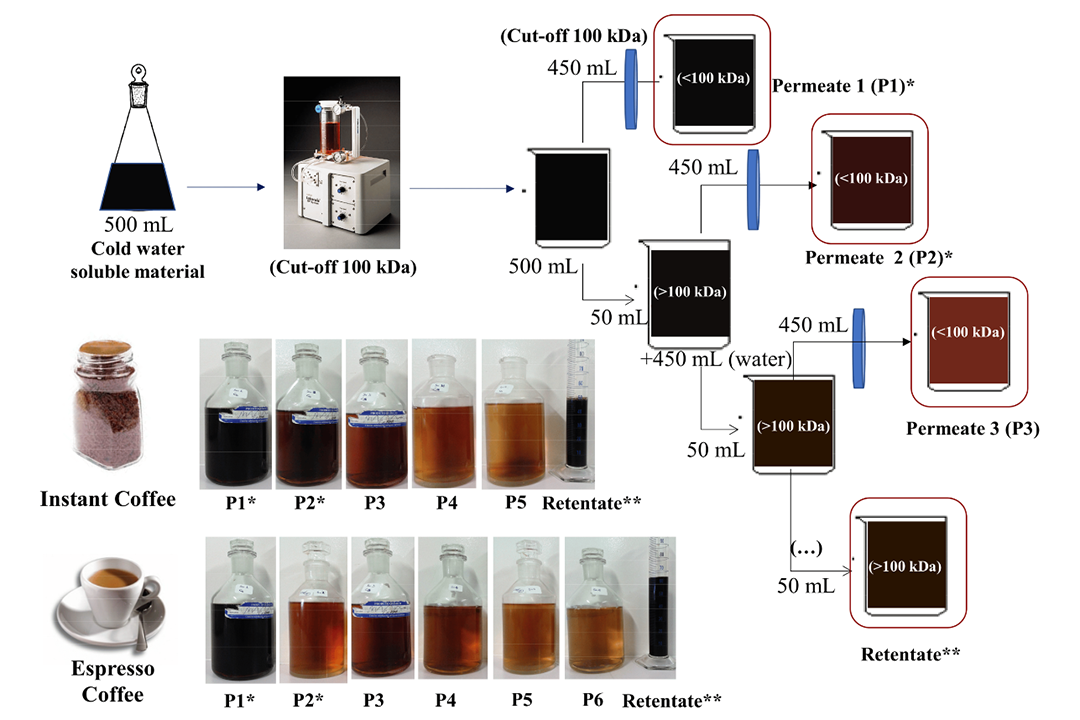
اگر اسیدها به عنوان بازهای مزدوج وجود داشته باشند، این اثر تقویت می شود، و بنابراین مطالعه ما نشان دهنده یک نمایش محافظه کارانه از اتصال ترکیبات قهوه به یون های محلول در آب است.
بر اساس آزمایشهای ترمودینامیکی ما، میتوان استدلال قانعکنندهای برای تبادل مطلوبCa2+ با Mg2+ برای افزایش بازده عصارهگیری، بدون کسری طعم قهوه، و مزیت اضافی حذف منبع رسوب آهک ارائه داد. ما همچنین بر این نتیجه شگفتانگیز تأکید میکنیم که Na+ بهطور ضعیف به اکثر ترکیبات خنثی موجود در دانههای قهوه متصل میشود، و نشان میدهد که آب غنی از سدیم، علاوه بر حذف منبع رسوبگذاری، هیچ سودی برای مصرفکننده ندارد. بنابراین، اگر انگیزه عصارهگیری بیشترین ترکیبات قهوه (یعنی قهوه فوری) باشد، آب غنی از Mg2+ مناسب ترین است. اگر انگیزه دستیابی به بهترین توازن طعم ها برای یک قهوه روشن برشت باشد، هر دو Ca2+و Mg2+ کار قابل مقایسه ای را انجام می دهند، با Mg2+ دارای ویژگی اضافی جلوگیری از تشکیل رسوب است.
لازم به ذکر است که هیچ ترکیب خاصی از آب وجود ندارد که با طعمهای یکسان از انواع متفاوت برشته کاری قهوهها عصارهگیری کند. در عوض، آبی وجود دارد که بیشترین توانایی عصارهگیری را دارد (یعنی غنی از کاتیون)، و طعم حاصل به تعادل بین کاتیون های موجود در محلول و مقدار بی کربنات موجود (که به عنوان بافر عمل می کند) بستگی دارد. علاوه بر این، هر دانه طوری برشته میشود که بهترین طعم خود را در دم آوری با آب مناسب برای آن درجه نشان میدهد. ما این نکته را تصدیق میکنیم و تأکید میکنیم که این کار نقش مهمی را که یونهای محلول در تسهیل فرآیند عصارهگیری بازی میکنند، روشن میکند.
آب تاثیرات بسیاری در عصاره گیری قهوه دارد. کاتیون های موجود در آب همانطور که اشاره شد اهمیت زیادی در کیفیت نهایی قهوه خواهند داشت. هدف ما در مجله رئیس در بخش تحقیقی, اشاره کردن به این موضوعات بطور تخصصی ادامه خواهد داشت. پس در مقالات بعدی با ما همراه باشید تا آگاهی خود را در قسمت مختلف زنجیره قهوه از کاشت تا عصاره گیری ارتقاء بخشیم.